تتجدد الأمعاء البشرية بوتيرة أسرع من أي نسيج آخر في الجسم، ففي غضون أيام قليلة فقط، تتكوّن خلايا جديدة تنشأ من خلايا جذعية متخصصة، ومع ذلك ومع تقدمنا في العمر، تتراكم في هذه الخلايا الجذعية تغيرات لاجينية (Epigenetic changes)، وهي علامات كيميائية على الحمض النووي تعمل كمفاتيح تتحكم في بقاء الجينات نشطة أو صامتة.
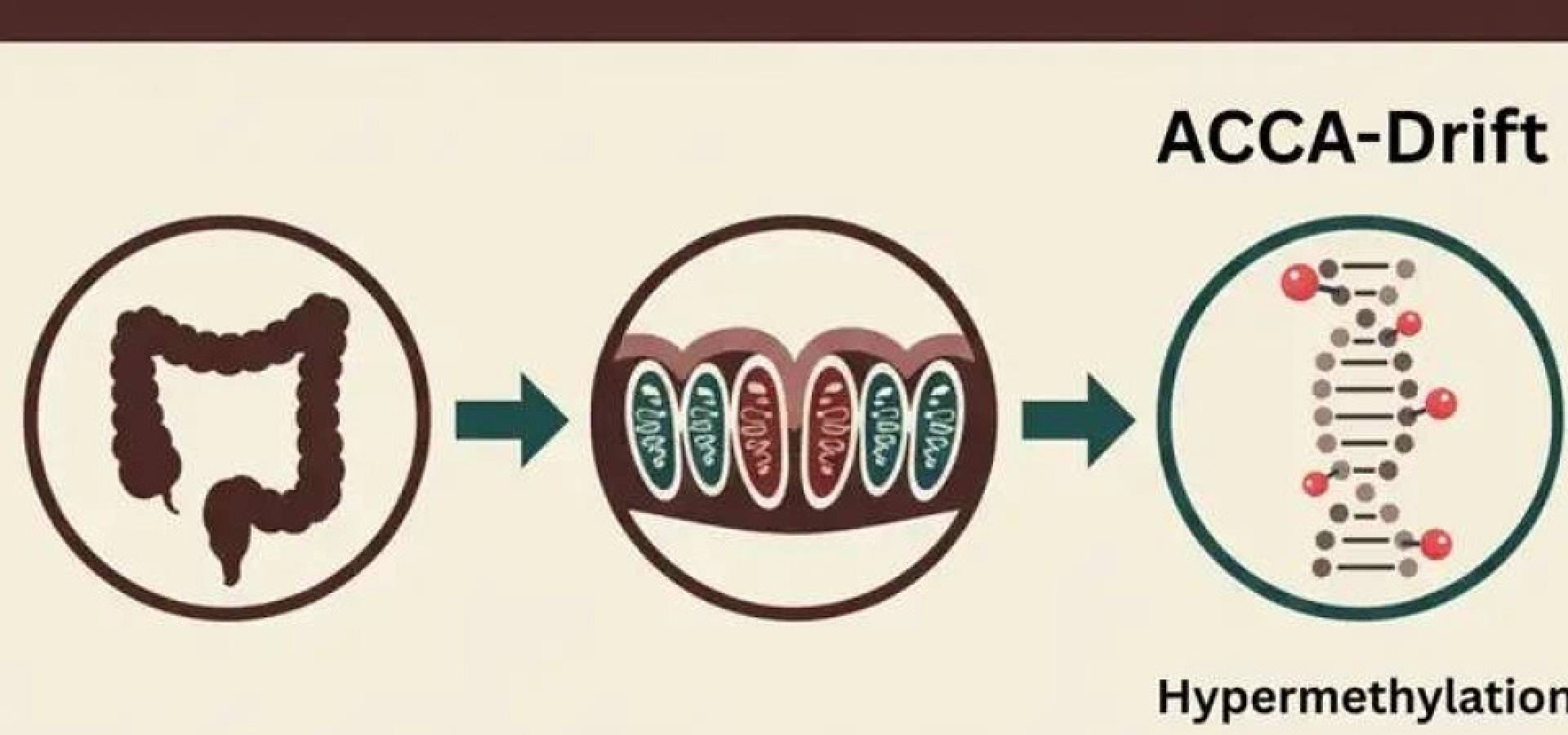
تكشف الدراسة الحديثة، التي نُشرت في مجلة Nature Aging وقادها فريق دولي بقيادة البروفيسور فرانشيسكو نيري من جامعة تورينو، أن التغيرات التي تحدث في الأمعاء ليست عشوائية، بل تتبع نمطا محددا يتطور بمرور الزمن. وقد سمى الباحثون هذا النمط باسم انحراف ACCA (اختصار: Aging- and Colon Cancer-Associated drift).
كيف يؤدي انحراف ACCA إلى إسكات الجينات؟
يشرح البروفيسور نيري، القائد السابق لمجموعة بحثية في معهد ليبنيز لأبحاث الشيخوخة، أن هذا النمط اللاجيني يزداد وضوحا مع التقدم في العمر.
وتتأثر بشكل خاص الجينات التي تحافظ على توازن الأنسجة الصحية، بما في ذلك تلك التي تنظم تجدد الظهارة المعوية عبر مسار إشارات Wnt الحيوي. وقد وجد الباحثون أن هذا “الانحراف” يظهر ليس فقط في الأمعاء المتقدمة في العمر، بل أيضاً في جميع عينات سرطان القولون تقريبا، مما يشير إلى أن شيخوخة الخلايا الجذعية تهيّئ بيئة ملائمة لنشوء السرطان.
بُقَع الشيخوخة: مناطق مختلفة تتقدم في العمر بوتيرة مختلفة
من أبرز نتائج الدراسة أن انحراف ACCA لا يتوزع بشكل متساوٍ في الأمعاء.
كل “جُبَيب” معوي (Crypt) – وهو أنبوب صغير في بطانة الأمعاء – ينشأ من خلية جذعية واحدة. وعندما تتعرض هذه الخلية لانحراف لاجيني، تنتقل هذه التغيرات إلى كامل الجُبَيب.
وتوضح الدكتورة آنا كريبلوفا: "مع مرور الوقت، تتشكّل مناطق واسعة في الأنسجة تحمل بصمة لاجينية متقدمة في العمر. ومن خلال عملية انقسام الجُبَيبات الطبيعية، تستمر هذه المناطق في الاتساع لسنوات طويلة."
وهذا يفسّر لماذا تحتوي أمعاء كبار السن على “فسيفساء” من الجُبَيبات الشابة وأخرى مُسنّة، ولماذا تكون بعض المناطق أكثر عرضة لتكوين خلايا متدهورة تعزز نمو السرطان.
نقص الحديد … السبب العميق وراء إسكات الجينات
كشفت الدراسة أيضا سببا جوهريا لهذه الانحرافات اللاجينية: اختلال استقلاب الحديد في الخلايا المعوية المسنّة.
أظهرت النتائج أن الخلايا الأكبر سنا:
تمتص كمية أقل من الحديد
وفي الوقت نفسه تُفرز كمية أكبر منه
مما يقلل disponibilty الحديد الثنائي (Fe²⁺) داخل نواة الخلية.
هذا النوع من الحديد ضروري لعمل إنزيمات TET، وهي مسؤولة عن إزالة فرط الميثلة على الحمض النووي. وعندما يتراجع الحديد المتوفر، تصبح إنزيمات TET غير قادرة على أداء وظيفتها.
وتشرح الدكتورة كريبلوفا: "عندما لا تحصل الخلايا على ما يكفي من الحديد، تبقى العلامات الخاطئة على الحمض النووي، وتفقد الخلايا قدرتها على إزالتها."
ينتج عن ذلك سلسلة من التأثيرات المتتابعة:
انخفاض نشاط إنزيمات TET
تراكم ميثلة الحمض النووي بشكل مفرط
إسكات الجينات المهمة
تفاقم الانحراف اللاجيني بسرعة أكبر.
الالتهاب وضعف مسار Wnt عوامل تُسرّع شيخوخة الأمعاء
أظهر الفريق البحثي أن الالتهابات الخفيفة المصاحبة للتقدم في العمر تعمل على تعزيز هذه العملية.
فالالتهاب:
يغيّر توزيع الحديد داخل الخلايا
يضغط على الاستقلاب
ويضعف مسار Wnt المسؤول عن إبقاء الخلايا الجذعية نشطة
تشكل هذه العوامل الثلاثة مجتمعة “مسرّعاً” قوياً للانحراف اللاجيني، مما يجعل الشيخوخة تبدأ في الأمعاء أبكر مما كان يُعتقد.
هل يمكن إبطاء هذا الانحراف أو عكسه؟
رغم تعقيد الآلية، تحمل الدراسة جانباً مشجعاً.
نجح الباحثون في إبطاء أو عكس الانحراف اللاجيني في نماذج عضوية مصغرة (Organoids) مشتقة من الخلايا الجذعية المعوية، وذلك عبر:
1. استعادة إدخال الحديد إلى الخلايا
2. أو تنشيط مسار Wnt بشكل موجّه
أدت هذه التدخلات إلى:
زيادة نشاط إنزيمات TET
إزالة الميثلة الزائدة
إعادة تنشيط الجينات الصامتة
وقالت الدكتورة كريبلوفا: "هذا يعني أن الشيخوخة اللاجينية ليست حالة نهائية وثابتة. ولأول مرة نرى إمكانية تعديل العوامل العميقة التي تتحكم في الشيخوخة على مستوى النواة نفسها."