كشف علماء من University of Tokyo عن آلية عمل فريدة لمركب طبيعي يسمى yaku’amide B، تم العثور عليه في إسفنج بحري يعيش في أعماق المحيط بالقرب من Yakushima Island.
ويتميز هذا المركب بخصائص قوية مضادة للأورام، حيث يمكنه ليس فقط إضعاف الخلايا السرطانية بل أيضًا منع انتشارها إلى أجزاء أخرى من الجسم. وقد نُشرت نتائج الدراسة في مجلة Journal of the American Chemical Society العلمية.
لغز علمي حول فعالية المركب
لفترة طويلة، لاحظ العلماء أن مركب yaku’amide B يمتلك قدرة استثنائية على إيقاف حركة الخلايا السرطانية. لكن الآلية الدقيقة التي يعمل بها ظلت غير واضحة.
في البداية اعتقد الباحثون أن المركب يؤثر فقط على الميتوكوندريا، وهي الأجزاء المسؤولة عن إنتاج الطاقة داخل الخلايا. إلا أن هذا التفسير لم يكن كافيًا لفهم سبب قدرته الكبيرة على منع انتشار الخلايا السرطانية.
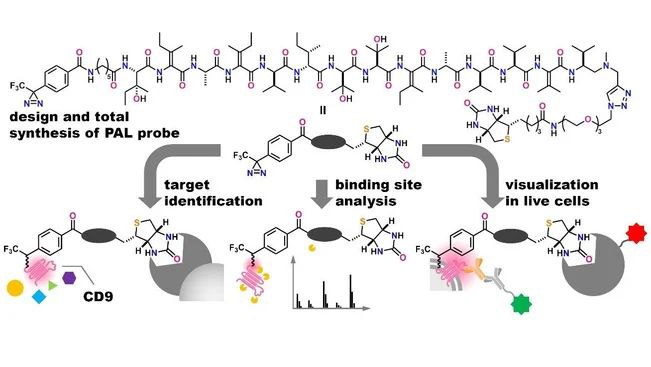
ولكشف هذا اللغز، استخدم العلماء تقنية متقدمة تُعرف باسم الوسوم الضوئية التفاعلية، والتي تسمح بتحديد الجزيئات التي يتفاعل معها الدواء داخل الخلية في لحظات قصيرة جدا.
ضربة مزدوجة للخلايا السرطانية
أظهرت النتائج أن مركب yaku’amide B يهاجم الخلايا السرطانية عبر آليتين متزامنتين:
1. تدمير بروتين مرتبط بانتشار السرطان
قبل أن يؤثر المركب على إنتاج الطاقة في الخلية، يقوم بالارتباط ببروتين غشائي يسمى CD9 protein.
ويعد هذا البروتين مؤشرا مهما للخلايا السرطانية الجذعية العدوانية التي غالبا ما تكون مسؤولة عن عودة المرض وانتشاره. وعند ارتباط المركب بهذا البروتين، يبدأ داخل الورم الخبيث عملية تحلل سريعة تؤدي إلى تدميره.
2. تعطيل إنتاج الطاقة في الخلية
في الوقت نفسه، يخترق المركب الميتوكوندريا داخل الخلية ويعطل إنزيما أساسيا يسمى ATP synthase المسؤول عن إنتاج الطاقة.
وبذلك تفقد الخلايا السرطانية مصدر الطاقة اللازم للنمو والتكاثر.
كيف يمنع المركب انتشار الأورام؟
بفضل هذا التأثير المزدوج:
تفقد الخلايا السرطانية قدرتها على إنتاج الطاقة اللازمة للنمو.
يتم تدمير البروتينات السطحية المسؤولة عن حركة الخلايا وانتشارها.
هذا يعني أن الورم لا يستطيع التكيف أو الانتشار إلى الأنسجة المجاورة، وهو ما يقلل بشكل كبير من فرص تكوين النقائل السرطانية (Metastases).
خطوة مهمة نحو تطوير أدوية جديدة للسرطان
وفقا للباحثين، تعد هذه المرة الأولى عالميا التي يتم فيها إثبات أن مركبًا طبيعيًا يمكنه التسبب مباشرة في تحلل بروتين CD9 المرتبط بانتشار السرطان.
ويفتح هذا الاكتشاف المجال أمام تطوير جيل جديد من الأدوية المضادة للسرطان، حيث يمكن للعلماء تصميم نسخ صناعية مشابهة لهذا المركب تستهدف الخلايا السرطانية بطرق متعددة في الوقت نفسه.
وقد يساعد هذا النهج في تطوير علاجات أكثر فعالية للحد من نمو الأورام ومنع انتشارها داخل الجسم.