كشفت دراسة علمية جديدة الآلية الخفية التي تستخدمها بكتيريا معوية شائعة لإتلاف خلايا القولون، في اكتشاف أنهى لغزًا حيّر العلماء لأكثر من 15 عاما.
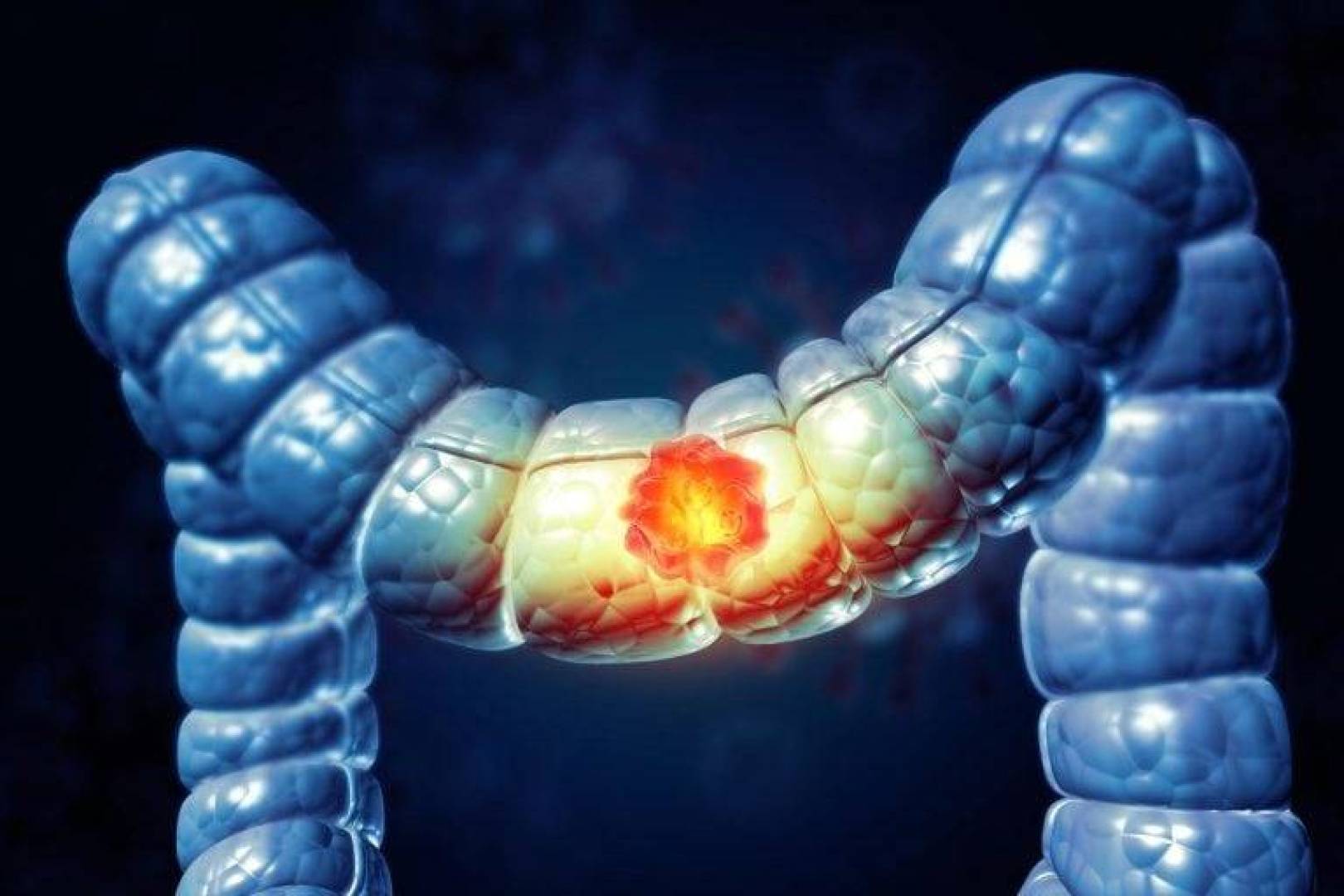
وكان الباحثون قد توصلوا منذ دراسة بارزة نُشرت عام 2009 إلى أن بكتيريا Bacteroides fragilis الموجودة في الأمعاء يمكن أن تعزز نمو أورام القولون التي قد تؤدي لاحقا إلى الإصابة بسرطان القولون والمستقيم. وتقوم هذه البكتيريا بإفراز سم يؤدي إلى إتلاف بطانة القولون، لكن الطريقة الدقيقة التي يلتصق بها السم بخلايا القولون ظلت غير معروفة حتى الآن.
تحديد المستقبل المسؤول عن ارتباط السم بالخلايا
قاد فريق بحثي من مركز جونز هوبكنز كيميل للسرطان ومعهد بلومبرغ-كيميل للعلاج المناعي للسرطان وكلية الطب بجامعة جونز هوبكنز الدراسة الجديدة، والتي نُشرت في مجلة Nature العلمية.
ووجد الباحثون أن السم البكتيري المعروف باسم BFT يحتاج أولا إلى الارتباط بمستقبل خلوي يسمى claudin-4 حتى يتمكن من إلحاق الضرر بالخلايا.
وحصل البحث على تمويل جزئي من المعاهد الوطنية للصحة الأمريكية.
وقالت الباحثة الرئيسية في الدراسة، الدكتورة سينثيا سيرز، أستاذة العلاج المناعي للسرطان في جامعة جونز هوبكنز، إن الفريق حاول عدة مرات على مدار سنوات تحديد هذا المستقبل، مؤكدة أن فهم طريقة عمل السموم البكتيرية قد يفتح المجال أمام وسائل جديدة للكشف والعلاج لأمراض مرتبطة بها، مثل الإسهال وسرطان القولون والتهابات مجرى الدم.
تطوير طُعم جزيئي لمنع الضرر
ساعد هذا الاكتشاف الباحثين بالفعل على تطوير ما وصفوه بـ"الطُعم الجزيئي"، وهو نسخة بديلة من المستقبل الخلوي تمكنت من تعطيل التأثيرات الضارة للسم في تجارب أُجريت على الفئران.
وأظهرت النتائج أن هذه الطريقة قد تمثل وسيلة مستقبلية لمنع الأضرار التي تسببها بكتيريا Bacteroides fragilis داخل القولون.
بكتيريا شائعة لدى الأصحاء
توجد بكتيريا Bacteroides fragilis لدى ما يصل إلى 20% من الأشخاص الأصحاء، لكنها تُعرف بقدرتها الكبيرة على تحفيز التهابات القولون والمساهمة في تكوين الأورام.
وأظهرت أبحاث سابقة أجراها مختبر الدكتورة سيرز أن السم البكتيري BFT يسبب التهابات مزمنة في الأمعاء من خلال قطع بروتين يسمى E-cadherin، وهو بروتين أساسي للحفاظ على الحاجز الواقي لبطانة القولون.
وفي دراسة سابقة نُشرت في مجلة Nature Medicine، أثبت الباحثون أن نشاط السم يساهم في تطور أورام القولون، إلا أن السم لم يكن يرتبط مباشرة ببروتين E-cadherin، ما دفع العلماء للاعتقاد بوجود آلية أخرى غير مكتشفة.
تقنية تعديل الجينات كشفت الحلقة المفقودة
للكشف عن هذه الآلية، قاد الباحث ماكسويل وايت، وهو طالب دكتوراه في الطب والعلوم، تجربة واسعة باستخدام تقنية تعديل الجينات CRISPR بالتعاون مع باحثين من كلية الطب بجامعة هارفارد.
واعتمدت التجربة على تعطيل الجينات بشكل منهجي داخل خلايا بطانة القولون، ما أدى إلى اكتشاف أن مستقبل claudin-4 يمثل الحلقة الأساسية في عملية ارتباط السم بالخلايا.
وعندما تمت إزالة هذا المستقبل، لم يعد السم قادرا على الالتصاق بالخلايا، وبقي بروتين E-cadherin دون تأثر.
وقال وايت إن تشغيل التجربة والتحقق من دقتها استغرق وقتًا طويلًا، لكن النتائج أوضحت بشكل قاطع أن claudin-4 هو المستقبل الرئيسي المسؤول عن ارتباط السم.
آلية ارتباط غير متوقعة
أوضح الباحثون أن هذا الاكتشاف كان مفاجئا، لأن كثيرًا من العلماء كانوا يتوقعون أن يكون المستقبل المسؤول عبارة عن بروتين إشارات خلوية، وهو ما لا ينطبق على claudin-4.
كما أشار الفريق إلى أنهم لم يعثروا في الدراسات السابقة على سم آخر يعمل بهذه الطريقة، إذ إن معظم الإنزيمات المحللة للبروتينات ترتبط مباشرة بأهدافها بدلا من الارتباط أولا بمستقبل منفصل.
إثبات الارتباط المباشر بين السم والمستقبل
وللتأكد من وجود تفاعل مباشر بين السم والمستقبل، تعاون فريق جونز هوبكنز مع علماء أحياء بنيوية من معهد البيولوجيا الجزيئية في برشلونة.
وأظهرت التحليلات الفيزيائية الحيوية أن السم BFT ومستقبل claudin-4 يشكلان مركبا قويا بنسبة ارتباط واحد إلى واحد داخل أنبوب الاختبار، وهو أول دليل مباشر على هذا التفاعل.
نجاح التجارب على الفئران
وسع الباحثون نطاق الدراسة إلى أنظمة حية من خلال تجارب على الفئران بالتعاون مع مختبرات تابعة لكلية الطب بجامعة هارفارد.
وقام الفريق بتطوير نسخة خداعية قابلة للذوبان من مستقبل claudin-4، بحيث يرتبط السم بهذه النسخة البديلة بدلًا من خلايا القولون الحقيقية.
وأظهرت النتائج نجاح هذه الاستراتيجية في حماية الفئران من الأضرار الناتجة عن السم البكتيري.
وأكد الباحثون أن هذه الطريقة يمكن تطويرها مستقبلا باستخدام جزيئات دوائية صغيرة أو علاجات حيوية أكثر كفاءة من الناحية الدوائية.
أسئلة علمية ما تزال دون إجابة
ورغم هذا التقدم العلمي، أشار العلماء إلى أن هناك سؤالا مهما لا يزال دون إجابة، إذ لم يتمكنوا حتى الآن من تحديد البنية الدقيقة الكاملة للتفاعل بين السم BFT ومستقبل claudin-4 على المستوى الجزيئي.
كما أوضحوا أن أنظمة الذكاء الاصطناعي الحالية، مثل AlphaFold، لم تتمكن حتى الآن من حل تفاصيل هذا التفاعل بشكل كامل.