كشف باحثون من Yale School of Medicine عن أداة تحليلية جديدة تساعد في فهم سبب اختلاف استجابة مرضى السرطان رغم تشابه التشخيص الطبي بينهم.
وأوضح العلماء أن الورم السرطاني لا يتحدد فقط بالطفرات المكتسبة مع الوقت، بل يتأثر أيضا بمزيج معقد من الاضطرابات الوراثية الموروثة والتغيرات الجينية المكتسبة التي تختلف من شخص لآخر.
ونُشرت نتائج الدراسة في مجلة Genome Medicine.
لماذا تختلف نتائج المرض بين المرضى؟
لطالما لاحظ الأطباء أن مرضى يمتلكون النوع نفسه من السرطان وفي المرحلة ذاتها قد يواجهون نتائج مختلفة تماما من حيث تطور المرض والاستجابة للعلاج.
وقال الباحث Lajos Pusztai، أستاذ طب الأورام في جامعة ييل، إن كل حالة سرطان تُعد فريدة بيولوجيا، لأن كل مريض يحمل اضطرابات جينية خاصة به تؤثر في طريقة تطور الورم.
وأشار إلى أن جميع السرطانات تشترك في مسارات بيولوجية أساسية، لكن الاختلاف الحقيقي يكمن في حجم ونوع الخلل الذي يصيب هذه المسارات لدى كل شخص.
تطوير أداة CanSys لتحليل الأضرار الجينية
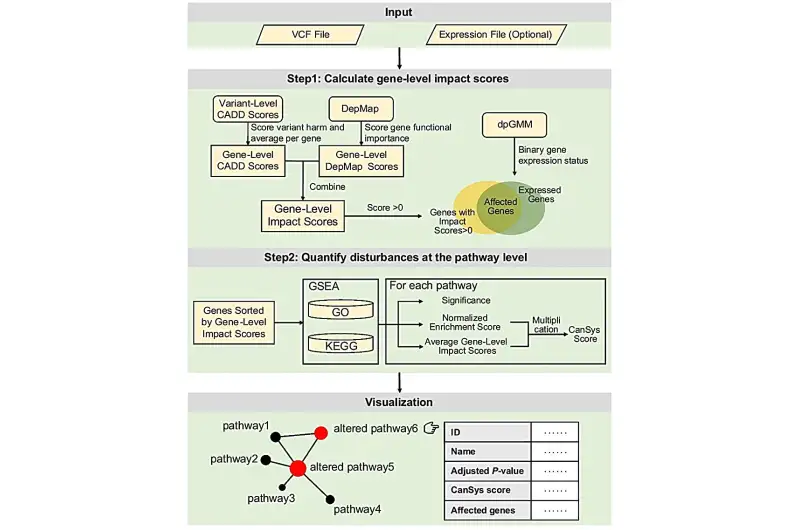
طوّر الفريق البحثي أداة مفتوحة المصدر تحمل اسم CanSys، وتهدف إلى إنشاء تقرير شخصي يوضح حجم الضرر البيولوجي داخل كل ورم سرطاني.
وتعتمد الأداة على سؤالين رئيسيين يتعلقان بكل جين داخل الورم:
مدى خطورة الطفرة الموجودة في الجين.
أهمية هذا الجين في بقاء الخلية السرطانية ونموها.
ولتحليل ذلك، استخدم الباحثون نظاما حاسوبيا يمنح كل طفرة جينية “درجة ضرر” توضح مدى تأثيرها على البروتينات التي ينتجها الجين.
كما استعانوا ببيانات منصة DepMap، التي تدرس تأثير تعطيل الجينات على بقاء الخلايا السرطانية عبر مئات السلالات الخلوية.
كيف تعمل الأداة الجديدة؟
بعد حساب التأثير الجيني لكل طفرة، قام الباحثون بربط النتائج بمسارات بيولوجية مرتبطة بالسرطان، مثل:
إصلاح الحمض النووي DNA.
تنظيم دورة انقسام الخلايا.
الحفاظ على التيلوميرات المسؤولة عن عمر الخلية.
ثم جرى جمع هذه التأثيرات في مؤشر شامل أطلق عليه اسم “درجة CanSys”، وهو مقياس يوضح حجم الاضطراب داخل النظام البيولوجي الكامل للورم.
وأوضح الباحثون أن الأداة لا تكتفي بتحليل خلل جين واحد فقط، بل تقيس الضرر الإجمالي الذي يصيب شبكات العمل الحيوية داخل الخلية السرطانية.
تحليل أكثر من 9 آلاف ورم سرطاني
اختبر الفريق أداة CanSys على أكثر من 9 آلاف عينة أورام تغطي 31 نوعا مختلفا من السرطان ضمن قاعدة بيانات The Cancer Genome Atlas.
وأظهرت النتائج أن نسبة كبيرة من مرضى السرطان يمتلكون اضطرابات وراثية موروثة تؤثر في آليات إصلاح الحمض النووي وتنظيم دورة الخلية.
لكن المفاجأة كانت أن هذه الاضطرابات ظهرت أيضا لدى أشخاص أصحاء لا يعانون من السرطان ضمن بيانات مشروع 1000 Genomes Project.
ما الذي يعنيه ذلك؟
يرى الباحثون أن كثيرا من البشر يولدون بخلل طفيف في بعض المسارات البيولوجية المرتبطة بالسرطان، لكن تطور المرض يعتمد على تراكم أضرار إضافية مع مرور الوقت.
وبحسب الدراسة، فإن الأشخاص الذين يمتلكون عددا أكبر من الاضطرابات الوراثية الموروثة قد يحتاجون إلى عدد أقل من الطفرات الإضافية حتى يبدأ السرطان بالتطور.
وقال Lajos Pusztai إن زيادة مستوى الخلل الوراثي الموروث قد تفسر سبب إصابة بعض الأشخاص بالسرطان في أعمار مبكرة مقارنة بغيرهم.
الذكاء الاصطناعي لتوقع خطر السرطان مستقبلا
يعمل فريق جامعة ييل حاليا على توسيع المشروع بالتعاون مع قاعدة بيانات UK Biobank التي تضم بيانات صحية وجينية لنحو 500 ألف شخص.
ويهدف الباحثون إلى تطوير نظام ذكاء اصطناعي قادر على حساب خطر الإصابة بالسرطان اعتمادًا على مجموع الاضطرابات الوراثية التي يولد بها الإنسان.
ويأمل الفريق أن تساعد هذه التقنية مستقبلا في تحسين برامج الفحص المبكر وتحديد الأشخاص الأكثر عرضة للإصابة بالمرض قبل ظهور الأعراض بسنوات.